വാർത്തകളിൽ ഇടംനേടിയത് എന്തുകൊണ്ട്?
അപൂർവ ജനിതക വൈകല്യങ്ങൾ (rare genetic disorders) നിർണ്ണയിക്കുന്നതിനുള്ള ഒരു ഫസ്റ്റ്-ലൈൻ പരിശോധനയായി (first-line test) ജനിതകശാസ്ത്രജ്ഞരും (Geneticists) ക്ലിനിക്കുകളും ഹോൾ-എക്സോം സീക്വൻസിംഗിനെ (whole‑exome sequencing) കൂടുതലായി പിന്തുണയ്ക്കുന്നു. ജീനോമിൻ്റെ പ്രോട്ടീൻ-കോഡിംഗ് (protein-coding) ഭാഗം മാത്രം പരിശോധിക്കുന്നത് അകാരണമായ വികസന കാലതാമസങ്ങളോ ജന്മനായുള്ള വൈകല്യങ്ങളോ (congenital anomalies) ഉള്ള രോഗികൾക്ക് വേഗത്തിലും ചെലവ് കുറഞ്ഞതുമായ (cost-effective) ഉത്തരങ്ങൾ നൽകാൻ സഹായിക്കുമെന്ന് 2026 ഏപ്രിലിലെ പുതിയ ക്ലിനിക്കൽ മാർഗ്ഗനിർദ്ദേശങ്ങൾ (clinical guidelines) എടുത്തുകാണിക്കുന്നു.
പശ്ചാത്തലം
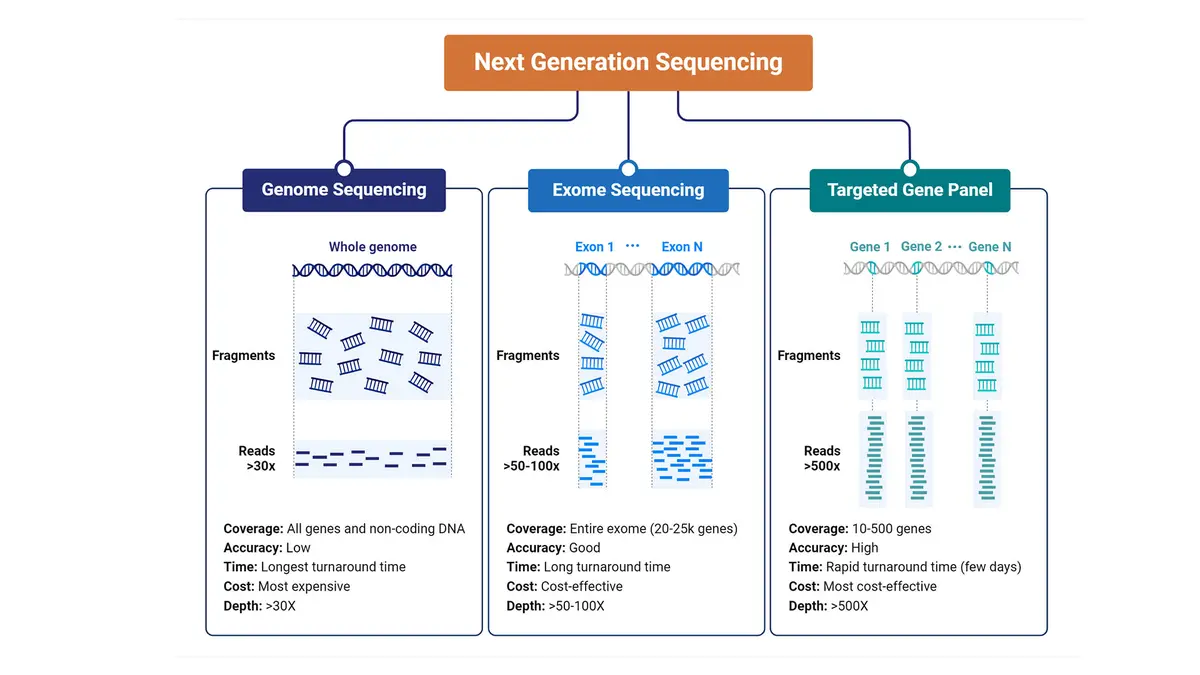
മനുഷ്യ ജീനോമിൽ ഏകദേശം 20,000 പ്രോട്ടീൻ കോഡിംഗ് ജീനുകൾ (protein-coding genes) അടങ്ങിയിരിക്കുന്നു. ഇവയുടെ എക്സോണുകൾ (exons) നമ്മുടെ ഡിഎൻഎയുടെ (DNA) രണ്ട് ശതമാനത്തിൽ താഴെ മാത്രമാണ്. എങ്കിലും രോഗമുണ്ടാക്കുന്ന വ്യതിയാനങ്ങളിൽ 80 ശതമാനത്തിലധികവും ഈ പ്രദേശങ്ങളിലാണ് കാണപ്പെടുന്നത്. ഹോൾ-എക്സോം സീക്വൻസിംഗ് (WES) ഈ കോഡിംഗ് വിഭാഗങ്ങളെ (coding segments) മാത്രം ക്യാപ്ചർ ചെയ്യുകയും സീക്വൻസ് ചെയ്യുകയും ചെയ്യുന്നു. ഹോൾ ജീനോം സീക്വൻസിംഗുമായി (WGS) താരതമ്യപ്പെടുത്തുമ്പോൾ, WES വളരെ കുറഞ്ഞ ഡാറ്റ മാത്രമേ സൃഷ്ടിക്കുന്നുള്ളൂ. അതിനാൽ വിശകലനം വേഗത്തിലും കൂടുതൽ താങ്ങാനാവുന്നതുമാക്കുന്നു, അതേസമയം അറിയപ്പെടുന്ന മിക്ക രോഗാണു വ്യതിയാനങ്ങളും (pathogenic variants) ഇത് ഉൾക്കൊള്ളുന്നു. ഒരു രോഗിയുടെ ഡിഎൻഎയിൽ നിന്നുള്ള എക്സോണുകൾ വർദ്ധിപ്പിക്കുകയും, ഉയർന്ന ത്രൂപുട്ട് പ്ലാറ്റ്ഫോമിൽ (high-throughput platform) അവയെ സീക്വൻസ് ചെയ്യുകയും, അപൂർവമായതോ ഹാനികരമായതോ ആയ മാറ്റങ്ങൾ തിരിച്ചറിയുന്നതിന് റഫറൻസ് ജീനോമുകളുമായി (reference genomes) ഫലങ്ങൾ താരതമ്യം ചെയ്യുകയും ചെയ്യുന്നതാണ് പ്രക്രിയ.
പ്രയോഗങ്ങളും ഗുണങ്ങളും (Applications and advantages)
- ഡയഗ്നോസ്റ്റിക് യീൽഡ് (Diagnostic yield): മോണോജെനിക് അസുഖങ്ങൾ (monogenic disorders) സംശയിക്കുന്ന 20-50 ശതമാനം രോഗികൾക്കും WES ഒരു ജനിതക രോഗനിർണയം നൽകിയേക്കാം. ഇത് ടാർഗെറ്റഡ് ജീൻ പാനലുകളേക്കാളോ (targeted gene panels) ക്രോമസോമൽ മൈക്രോഅറേ (chromosomal microarray) ടെസ്റ്റുകളേക്കാളോ മികച്ച പ്രകടനം നൽകുന്നു.
- ചെലവ് കുറഞ്ഞത്: പ്രവർത്തനക്ഷമമായ മിക്ക വേരിയൻ്റുകളും കാണപ്പെടുന്ന ജീനോമിൻ്റെ രണ്ട് ശതമാനത്തിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കുന്നതിലൂടെ, ഹോൾ ജീനോം സീക്വൻസിംഗുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ WES സീക്വൻസിംഗ് ചെലവുകളും (sequencing costs) ഡാറ്റ വിശകലന ഭാരവും കുറയ്ക്കുന്നു.
- വിപുലമായ ഉപയോഗം (Broad utility): വികസന കാലതാമസം, ബൗദ്ധിക വൈകല്യം (intellectual disability), അപസ്മാരം, ജന്മനായുള്ള വൈകല്യങ്ങൾ എന്നിവ പോലുള്ള ജനിതകപരമായി വൈവിധ്യമുള്ള (genetically heterogeneous) അവസ്ഥകൾക്ക് ഇത് പ്രത്യേകിച്ചും ഉപയോഗപ്രദമാണ്, അവിടെ പല ജീനുകൾ സമാന ലക്ഷണങ്ങൾ ഉണ്ടാക്കാം.
- ഗവേഷണ ഉപകരണം: പുതിയ രോഗ ജീനുകൾ കണ്ടെത്താനും മ്യൂട്ടേഷനുകൾ (mutations) പ്രോട്ടീൻ്റെ പ്രവർത്തനത്തെ എങ്ങനെ ബാധിക്കുന്നുവെന്ന് മനസ്സിലാക്കാനും WES ഗവേഷകരെ സഹായിക്കുന്നു, ഇത് ടാർഗെറ്റഡ് തെറാപ്പികൾ (targeted therapies) വികസിപ്പിക്കുന്നതിന് സംഭാവന നൽകുന്നു.
പരിമിതികൾ (Limitations)
- അപൂർണ്ണമായ കവറേജ്: WES ജീനോമിൻ്റെ റെഗുലേറ്ററി അല്ലെങ്കിൽ ഇൻട്രോണിക് (intronic) പ്രദേശങ്ങൾ പരിശോധിക്കുന്നില്ല. കൂടാതെ ജീൻ എക്സ്പ്രഷനെ ബാധിക്കുന്ന ഘടനാപരമായ പുനർക്രമീകരണങ്ങളോ കോഡിംഗ് അല്ലാത്ത മ്യൂട്ടേഷനുകളോ വിട്ടുപോയേക്കാം.
- വേരിയൻ്റ് ഇൻ്റർപ്രെട്ടേഷൻ (Variant interpretation): കണ്ടെത്തിയ പല മാറ്റങ്ങൾക്കും അനിശ്ചിതമായ പ്രാധാന്യമുണ്ട്, അവ രോഗത്തിന് കാരണമാകുമോ എന്ന് നിർണ്ണയിക്കാൻ ക്ലിനിക്കൽ കോറിലേഷനും ഫംഗ്ഷണൽ സ്റ്റഡീസും (functional studies) ആവശ്യമാണ്.
- നൈതിക പരിഗണനകൾ: സീക്വൻസിംഗ് രോഗിയുടെ നിലവിലെ അവസ്ഥയുമായി ബന്ധമില്ലാത്ത ആകസ്മിക കണ്ടെത്തലുകൾ (incidental findings) വെളിപ്പെടുത്തിയേക്കാം. ഇത് സമ്മതത്തെയും കൗൺസിലിംഗിനെയും കുറിച്ചുള്ള ചോദ്യങ്ങൾ ഉയർത്തുന്നു.
ഉപസംഹാരം
ആയിരക്കണക്കിന് ജീനുകളിൽ ഒരേസമയം തിരയുന്നത് സാധ്യമാക്കുന്നതിലൂടെ ഹോൾ എക്സോം സീക്വൻസിംഗ് മെഡിക്കൽ ജനിതകശാസ്ത്രത്തെ മാറ്റിമറിക്കുകയാണ്. ക്ലിനിക്കൽ വിലയിരുത്തലിനൊപ്പം (clinical assessment) വിവേകപൂർവ്വം (judiciously) ഉപയോഗിക്കുന്നത്, രോഗനിർണ്ണയ സമയദൈർഘ്യം കുറയ്ക്കാനും വ്യക്തിഗതമാക്കിയ ചികിത്സാ തന്ത്രങ്ങൾ (personalised treatment strategies) തയ്യാറാക്കാനും സഹായിക്കും.